-
Вход в личный кабинет - Вход в личный кабинет
- Обратная связь
- Подписка на рассылку
- Карта сайта
| Статьи |
Химически чистая вода H2O бесцветна, не имеет запаха и вкуса, в относительно толстом слое кажется окрашенной в голубоватый цвет.
Молекула воды состоит из двух одновалентных ионов водорода H+ и двухвалентного ионы кислорода О2—, которые расположены в вершинах равнобедренного треугольника. Угол у вершины треугольника, занятый ионом кислорода, равен 104,5°, длина связи О—Н равна 0,096 нм, расстояние между ионами Н+ равно 0,15 нм, размер молекулы воды считается близким к 0,28 нм (рис. 1.1).
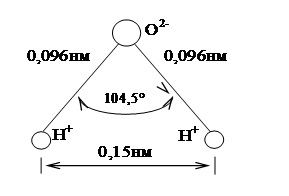 |
| Рис. 1.1. Простейшая схема молекулы воды |
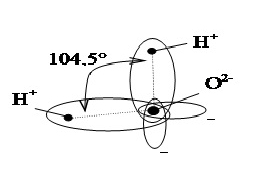
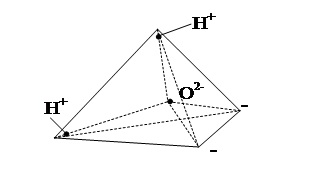
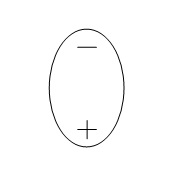
Ближе к реальности представление молекулы H2O в форме пространственной фигуры — тетраэдра с двумя положительными вершинами на ионах водорода Н+ и двумя отрицательными вершинами на вытянутых электронных орбитах иона кислорода (рис. 1.2). Иногда упрощенно молекулы воды изображают в виде диполя (рис. 1.3), поскольку центры положительных и отрицательных зарядов не совпадают.
| 
| 
|
| Рис. 1.2. Представление молекулы воды в виде тетраэдра | Рис. 1.3. Представление молекулы воды в виде диполя | |
Особенностью молекул воды являются способность соединяться между собой в многозвенные ассоциаты за счет образования водородных связей (рис. 1.4).
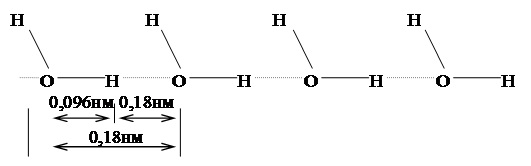 |
| Рис. 1.4. Схема образования водородных связей между молекулами воды |
Поскольку у молекулы имеются как бы четыре полюса электрических зарядов, то каждая молекула связывается с четырьмя другими молекулами, располагающимися также в вершинах тетраэдра (рис. 1.5).
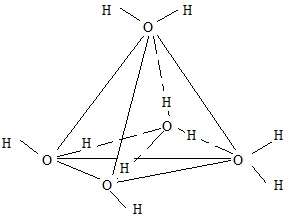 |
| Рис. 1.5. Пространственный ассоциат в виде тетраэдра из молекул воды |
Эти пятизвенные тетраэдры частично соединяются между собой, образуя более сложные пространственные структуры. Ассоциаты не являются устойчивыми постоянными пространственными элементами структуры воды. Вследствие теплового движения ориентация молекул изменяется, что приводит к распаду существующих ассоциатов и образованию новых. Продолжительность жизни ассоциатов предполагается близкой к 10—12—10—11 секунд. Столь быстрое установление и разрушение пространственных упорядоченных элементов делает структуру воды исключительно изменчивой («мерцающей»), а упорядочение носит статистический характер.
Степень ассоциированности зависит от температуры воды. Полностью все молекулы ассоциированы между собой в единую жесткую пространственную структуру только во льду, причем при температуре ниже —183° С. При более высокой температуре часть водородных связей разрушается; считается, что вблизи температуры плавления (0° С) разрушаются 9–16% общего количества водородных связей, а при 40° С — примерно половина. При переходе в газообразное состояние (в пар) разрушаются практически все водородные связи, очень небольшая часть молекул воды соединена в двойные агрегаты (дигидроли). Изменение степени ассоциированности оказывает столь заметное влияние на свойства воды, что, по мнению некоторых специалистов, воду при 25—75°С и воду вблизи 0°С можно рассматривать как два различных по своей природе растворителя. Жидкую воду можно представить состоящей из областей двух видов — «льдоподобных» с ассоциированными молекулами и «плотноупакованных» со свободными отдельными молекулами. Такие области, включающие 102–103 молекул, постоянно разрушаются и вновь возникают.
Энергия водородных связей составляет около 18,9 кДж/моль (4,5 ккал/моль), она значительно меньше энергии химической связи, составляющей более 100 кДж/моль. В то же время эта энергия превышает энергию вандервальсовых сил (9,6 кДж/моль) и энергию теплового движения молекул (около 2,5 кДж/моль при 27° С). Энергия образования молекул воды из водорода и кислорода представляет собой достаточно большую величину — 242 кДж/моль, что обусловливает высокую устойчивость молекул. Вода не изменяется под действием большинства соединений, которые растворяет, и считается инертным растворителем.
Вода имеет большую диэлектрическую проницаемость, кроме того ее молекулы представляют собой диполи, поэтому обладает высокой растворяющей способностью по отношению к полярным соединениям из-за снижения межатомных и межмолекулярных сил. Ионы растворенных веществ размещаются в структуре воды или в ее полостях, либо замещая молекулы Н2О. В любом случае они вызывают изменение структуры воды: во-первых, из-за несовпадения размеров иона и молекулы H2O, во-вторых, из-за изменения ориентации молекул Н2О вследствие влияния иона. Крупные слабозаряженные ионы разрушают структуру воды. Небольшие высокозаряженные ионы способствуют структурообразованию в воде, правда, эти структуры могут отличаться от характерной для воды льдоподобной структуры. Однако все эти эффекты справедливы до температуры 40—50°С, при более высокой температуре все ионы способствуют упрочнению структуры воды.
Эффект разрушения — упрочнения структуры сказывается на таких параметрах, как вязкость, диффузия и, соответственно, зависящих от них явлений очистки воды (коагуляция, осаждение и т.д.)
Образование структур из дипольных молекул воды вокруг ионов растворимых веществ или других заряженных частиц носит название гидратации. Чем выше заряд иона и чем меньше его размеры, тем сильнее он гидратируется, тем большее количество молекул воды входит в гидратную оболочку иона. Катионы, как правило, гидратируются сильнее, чем анионы.
Образование водородных связей и структурирование обусловливают многие исключительные свойства воды, отличающие ее от водородных соединений соседних элементов (аномалии воды). Ниже приводятся основные параметры воды.
| Диэлектрическая проницаемость E (при 20° С) | 81 |
| Электрический дипольный момент | 1,84 Дебая |
| Удельная электропроводность обессоленной воды | ~4•10-8ом-1см-1 |
| Плотность при 0° С | 0,9998 кг/дм³ |
| Эбуллиоскопическая константа (повышение температуры кипения при растворении 1 моля вещества в 1000 г воды) | 0,52° C |
| Криоскопическая константа (снижение температуры плавления при растворении 1 моля вещества в 1000 г воды) | 1,86° C |
| Температура плавления (замерзания) | 0° С |
| Температура кипения | 100° С |
| Теплота плавления | 335 кДж/кг (80 ккал/кг) |
| Теплота испарения | 2263 кДж/кг (539 ккал/кг) |
| Удельная теплоемкость | 4,19 кДж/кг (1 ккал/кг) |
| Кинематическая вязкость при t = | 0° С 1,79 сст
20° С 1,01 сст 40° С 0,66 сст |
| Поверхностное натяжение при 20° С | 0,07275 н/м |
| Критические константы: температура, выше которой вода не может быть сжижена путем изотермического сжатия | 374° С |
| давление | 218,5 атм |
| плотность | 0,324 кг/дм³ |
| Давление пара при температуре: | 0° С 4,6 мм. рт. ст.
20° С 17,5 мм. рт. ст. 40° C 55,1 мм. рт. ст. 100° С 760 мм. рт. ст.(1 атм) 120° С 1,96 атм 150° C 4,70 атм |


